☆フラーレンと超分子
「超分子化学」(Supramolecular chemistry)という分野があります。正確な定義はかなり難しいのですが、まあ筆者流に噛み砕いて言ってしまえば「いくつかの分子やイオンが組み合わさることによって発揮される、ひとつの分子では見られないような面白い機能を研究する分野」ということになります。
この定義からすれば、非常に多くの化合物がこれにあてはまることになります。他の分子を取り込むクラウンエーテルやシクロファンなどもそうですし、タンパク質がいくつか集まった複合体なども超分子に含めることができます。もっといえば分子が寄り集まってできる細胞も超分子と呼べますし、人間の体だって分子が集まって複雑な機能を発揮している以上、超分子の一種であるということも可能です。


それはともかく、このジャンルでは当美術館にふさわしい美しい分子が数多く作り出されています。今回は特に美しい素材、フラーレンを用いたよりすぐりの超分子たちをお目にかけることにしましょう。
実はフラーレンを超分子化学の材料として使った研究は、すでにこのページでも何度か取り上げています。例えばRubinや小松らによって作り出された穴あきフラーレンは、フラーレンをホスト分子として使った例です。
しかしこの分野では、フラーレンをゲスト分子(大きな分子に取り込まれる方の分子)として使っている例がほとんどです。フラーレンは凹凸のない球体であり、しかも他の分子と引き合いやすい「π電子」がその表面を覆っています。要するにフラーレンは糊でべたべたのボールのようなもので、適当な大きさの穴があればすぐにそこにはまり込んで、安定な超分子錯体を作ってしまうのです。カリックスアレンの項で挙げた錯体はまさにその例です。
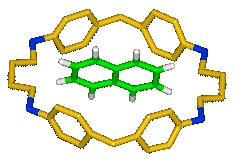
以前シクロファンの項で取り上げた「ナノリング」もフラーレンを取り込む環状分子ですが、最近さらに外側の環が2重になった「タマネギ型錯体」が登場しました。太陽系の模型を思わせる、非常に珍しい構造です。
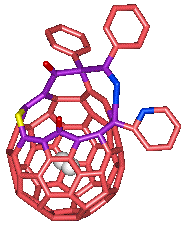
大きな正方形の分子であるポルフィリンもπ電子をたくさん持っており、フラーレンとも相互作用することが知られています。Boydらは2枚のポルフィリンをつなぎ合わせ、フラーレンを挟み込む錯体を合成しています。フラーレンに噛みつくような形のこのホスト分子に与えられた名は、ずばり「ジョーズポルフィリン」です。
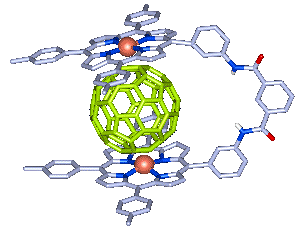
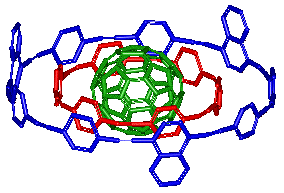
これを応用して相田らは面白いホスト分子を合成しています。2枚のポルフィリンを環につないだような下の分子は穴が少し大きすぎるためC60とは結合せず、もっと大きなフラーレンを選択的に捕まえます。下の図はC96を捕らえたところです。
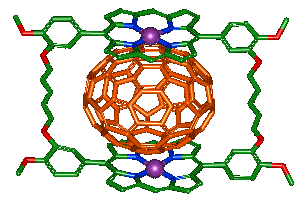
フラーレンは黒鉛にアーク放電を行って作ります。こうして得られる粗製フラーレンのほとんどはC60かC70で、これより大きなフラーレンは非常にわずかしかできないため取得が難しく、これまで研究があまり進んでいませんでした。この方法によれば簡単な操作で大型フラーレンを釣り上げることができ、精製もずっと簡単になりそうです。鎖やポルフィリンの構造をファインチューニングすればさらに認識精度を上げたり、C60の合成誘導体だけを捕まえるなどといったこともできそうで、今後面白い展開が期待できそうです。
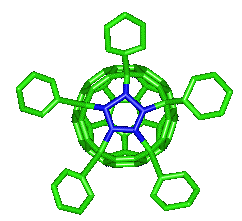
置換基の中央の5員環(下左、青色の部分)はマイナスの電荷を帯びています。ここには陽電荷を持つ鉄などのイオンが結合できます。こうしてできた分子(下左)はいわばフラーレン(バッキーボール)とフェロセン(下右)の「あいのこ」ということで、「バッキーフェロセン」という愛称がつけられました。ノーベル賞を獲得した2つの分子のハイブリッドということで、ちょっとした話題を呼んだ研究です。
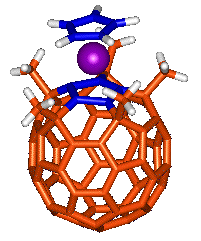
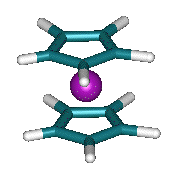
buckyferrocene(左)と通常のferrocene(右)。フェロセンの構造を解明したWilkinsonらは1973年にノーベル化学賞を受賞している。
またベンゼン環を5枚導入した下のような分子は、青い部分はマイナスの電荷を持つため水に溶けやすく、下半分は油に溶けやすい(水となじまない)という相反した性質を併せ持ちます。これは細胞膜の構成成分である脂肪酸などと同じ特徴です。
実はこの化合物も脂肪酸と同じく、フラーレンの底同士を合わせた2重膜となってお互いがびっしりと寄り集まり、直径34nmの中空の球を形成するのです。こうした事実は以前には全く予期されていなかった事柄であり、その性質と合わせて大きな注目を集めました。12,700分子が集まってできる「フラーレンベシクル」のCGは壮観そのもので、多くの学会誌の表紙や目次を飾っています(この画像は中村研究室のHPに掲載されていますので、ぜひご覧下さい)。
導入する置換基をフェニル基からビフェニル基(ベンゼンが2つつながったもの)に変えると、また全く違った世界が開けます。この分子ではビフェニルの傘の中に次のフラーレンが次々とはまり込み、ちょうどバドミントンのシャトルコックを積み重ねたような格好になるのです。
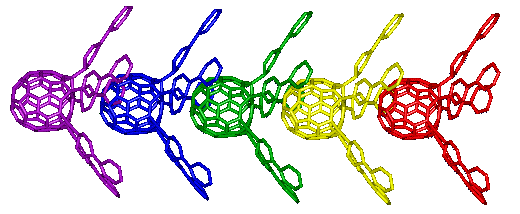
この分子は液晶としての性質を示します。普通の液体では分子があちこち好き勝手な方向を向いて動き回っていますが、特殊な形の分子の場合には液体でありながらある程度分子の方向が揃い、結晶に近い性質を示すことがあります。これが液晶です。電場によって液晶の並び方を制御し、背後の光を遮ることによって画像を表示するというのが、今あなたが見ている(かもしれない)液晶ディスプレイの原理です。
液晶になる分子は柱状のもの、円盤形のものなどが知られていましたが、こうした円錐形の分子が積み重なったタイプのものはこれが初めてです。それにしても一つの反応を突破口に次々と新しい世界を切り開いてみせる中村教授の手腕には、いつものことながら驚かされます。
現在工業的な窒素固定は「ハーバー=ボッシュ法」と呼ばれるプロセスで行われています。窒素と水素を1:3の割合で混合し、鉄触媒の存在下で200気圧、500度の条件で反応させることによりアンモニアを合成するものです。得られたアンモニアは食品や肥料、衣料など様々に形を変え、暮らしの中に入り込んでいます。
この方法は1906年に開発されて以来現在に至るまで使われ続けており、まさに20世紀化学工業の金字塔といえるものです。今では世界の食糧生産に関わる窒素の40%が、ハーバー=ボッシュ法に依存しているとまでいわれます。
空気から食料を作れるのですから極めて経済的――といいたいところですが、問題もないわけではありません。前述したようにハーバー=ボッシュ法は高温・高圧を必要とし、非常にエネルギーを食うプロセスなのです。式で書けば単純な反応である窒素固定を、なんとか室温・1気圧の条件下で実現したいというのは、この1世紀の間科学者たちの大きな夢でした。ごく最近になって干鯛ら及びSchrockらのグループがモリブデンなどの金属錯体を使ってこれを実現していますが、実用化までにはまだまだ遠い段階です。
実はこの何の関係もなさそうな分野に、なんとフラーレンが登場してきたのです。シクロデキストリンと呼ばれる、グルコースが8つ輪につながった有名なホスト化合物がありますが、フラーレンはこの分子とも1:2の錯体を作ることが知られています。
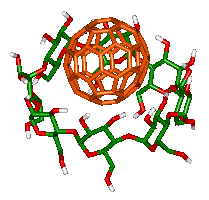
吉田・植村らのグループは、このフラーレン錯体に次亜硫酸ナトリウムを加え、光を当てるという実験を行いました。その結果、最高45%の収率で窒素からアンモニアが合成されることがわかったのです。金属などを一切使わず、常温常圧でこの反応が達成されたのはまさに画期的なことです。
フラーレンは次亜硫酸ナトリウムから電子を受け取って陰イオンになることが知られています。この電子が窒素分子に受け渡され、丈夫な三重結合を切断する働きをしているものと考えられます。シクロデキストリンはフラーレンを水に溶けやすくする他、余計な分子が近づいて反応を邪魔しないよう「ガード」する役目を果たしているのでしょう。
もちろんこの反応も効率的にはまだ極めて低く、すぐ実用に結びつくようなものではありません。しかしハーバー=ボッシュ法に代わる、環境に負荷をかけない新反応への大きな第一歩であるとはいえるでしょう。今後の展開が非常に楽しみな研究です。